
بیماری لی
| بیماری لی | |
|---|---|
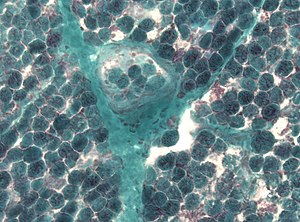 | |
| ردیابی تعداد زیادی «فیبر عضلانی قرمز ناصاف و خشن» در بیوپسی عضلانی | |
| تخصص |
عصبشناسی |
| طبقهبندی و منابع بیرونی | |
| آیسیدی-۱۰ | G31.8 |
| اُمیم | ۲۵۶۰۰۰ |
| دادگان بیماریها | 30792 |
| سمپ | D007888 |
بیماری لی (انگلیسی: Leigh disease) که با عناوینی چون «انسفالومیلوپاتی نکروزدهندهٔ تحت حاد خردسالان»، «سندرم لی»، «انسفالومیلوپاتی نکروزدهندهٔ تحت حاد نوزادان» و «انسفالومیلوپاتی نکروزدهندهٔ تحت حاد» (SNEM)، هم شناخته میشود، یک اختلال نادر ژنتیکی است که دستگاه عصبی مرکزی را تحت تأثیر خود قرار میدهد. این بیماری، نام خود را از عصبروانشناسِ بریتانیایی «آرچیبالد دنیس لی» (۱۹۹۸–۱۹۱۵) میگیرد که نخستین بار در سال ۱۹۵۱ میلادی، این بیماری را توصیف کرد.
علائم این بیماری تا قبل از یک سالگی ظاهر شده و ظرف چندین سال، منجر به مرگ میشود؛ اما احتمال دارد نخستین علائم بیماری، از سه ماهگی تا دو سالگی و حتی خیلی به ندرت، در سنین کودکی و نوجوانی یا حتی بلوغ آغاز شود. گاهی نیز این بیماری، در رحم مادر شروع میشود. علائم بیماریِ لی اغلب زمانی خود را نشان میدهد که انرژی سلولهای بدن در اثرِ واقعهای همچون عفونت یا جراحی، کاهش یابد. سیرِ رایج بیماری نیز به صورت عقبافتادگی سریعِ رشد و تکامل کودک است.
نوزادان مبتلا به این بیماری، علائمی همچون اسهال، استفراغ و دشواری در بلع دارند که به اختلال رشد کودک منجر میشود. در مراحل اول آن، نوزاد بیقرار است و بیشتر از حدِ معمول گریه میکند. در اغلب موارد، تشنج نیز وجود دارد. سطحِ اسید لاکتیکِ ادرار، مایع مغزی-نخاعی و خون بالاست که علت آن، «اسیدوز لاکتیک» است. با پیشرفت بیماری، دستگاه ماهیچهای در سرتاسر بدن دچار ضعف میشود و مغز توانای کنترل انقباضی بدن را از دست میدهد. هیپوتونی (کاهش تُن عضلانی)، دیستونی، آتاکسی (فقدان کنترل بروی حرکات عضلانی) در بیشتر این افراد دیده میشود. چشمها از جمله اعضایی هستند که بیش از بقیه، تحت تأثیر بیماری واقع شده و ماهیچههای چشمی، دچار ضعف و فلج و عدم کنترل شده و اُفتالموپلژی (ضعف یا فلچ چشم) و نیستاگموس (حرکات غیرارادی چشم) رخ میدهد. گاهی سیکاد چشمی (حرکات سریع چشم) هم پیش میآید.
قلب و ریه نیز ممکن است دچار نارسایی شوند. «کاردیومیوپاتی هایپرتروفیک» (ضخیمشدگی بخشی از دیواره قلب) محتمل و از دلایل مرگ این بیماران است. «هایپرتروفی غیرقرینهٔ دیوارهٔ بینبطنی» هم در این بیماران گزارش شدهاست. در کودکانی که در اثرِ بیماری لی، دچار نقص دیواره بینبطنی ناشی از «کمبود پیرووات دِهیدروژناز» هستند، پیشانی بلند و گوشهای بزرگ دیده میشود؛ اما نقایصِ ناحیهٔ چهره، جزء تظاهراتِ رایجِ بیماری لی نیست.
در مجموع، شایعترین علت مرگ این بیماران نارسایی تنفسی است. سایر علائمِ عصبیِ بیماری شاملِ نوروپاتی محیطی و از دسترفتنِ حس در اندامِ تحتانی به دلیلِ گرفتاری دستگاه عصبی محیطی است.
گاهی در این بیماران پرمویی هم دیده میشود که علت آن جهش در ژنِ «SURF1» است.
تاریخچه
این بیماری نخستین بار، در سال ۱۹۵۱ میلادی توسط «دنیس لی» توصیف شد و در سال ۱۹۵۴ آن را از «انسفالوپاتی ورنیکه» افتراق دادند. در سال ۱۹۶۸ میلادی، ارتباط آن با فعالیت میتوکندریها پیشنهاد شد؛ اما کشفِ رابطهٔ آن با جهشهای ژنی سیتوکروم اکسیداز سی و سایر پروتئینهای زنجیره انتقال الکترون تا سال ۱۹۷۷ میلادی به طول انجامید.
همهگیرشناسی
احتمال بروز سندرم لی در جمعیت عادی، ۱ از ۴۰۰۰۰ مورد تولدِ زنده است؛ اما در برخی جمعیتها، این بیماری شیوع بیشتری دارد. به عنوان مثال، در ناحیهٔ سگنه-لاک-سن-ژان در مرکز استان کبکِ کانادا، احتمالِ تقریبیِ بروز آن ۱ از ۲۰۰۰ نوزاد است.
اساس ژنتیکی
جهش در دیانای میتوکندریایی (mtDNA) و همچنین ۳۰ ژن در دیانای هستهای (از جمله ژن «SURF1» و چند فاکتور ساخت سیتوکروم اکسیداز سی) از جمله دلایلِ مطرح در ایجاد بیماری لی هستند.
احتمالاً اختلال در فسفریلاسیون اکسیداتیو که طی آن سلولهای بدن به ساخت منبع اصلی انرژی خود یعنی آدنوزین تریفسفات میپردازند، به دلیلِ جهش در دیانای میتوکندریایی یا ژنهایی در دیانای هستهای است. جهش ژنهای دیانای هسته، نقش مهمتری دارد، اما گاهی نمیتوان، نوعِ جهشِ ژنی را در افراد مبتلا، بهدقت مشخص کرد. در بیماری لی، از ۵ کمپلکسِ پروتئینی دخیل در فسفریلاسیون اکسیداتیو، ۴ پروتئین دچار اختلال میشود که یا به دلیل اشکالات ساختاری پروتئین است یا اشتباه در ترکیببندی این کمپلکسهای پروتئینی. به هر تقدیر، دلایل ژنتیکی بیماری هرچه که باشد، پروتئینهای دخیل در فسفریلاسیون اکسیداتیو نمیتوانند نقش کلیدی خود را ایفا کنند و به ویژه سلولهای حیاتی در ساقهٔ مغز و عقدههای قاعدهای مغز تحت تأثیر این واقعه قرار میگیرند. این تغییرات سبب میشود تا سلولها، دچار کاهش مزمن انرژی شده و در نهایت از بین بروند و بدین ترتیب، دستگاه عصبی مرکزی و عملکرد حرکتی آن دچار اختلال میشود. قلب و عضلات بدن نیز که عموماً نیازمند مقادیر زیاد انرژی هستند، دچار مرگ سلولی تدریجی میشوند.
انواع
- جهشهای دیانای میتوکندری
۲۰ تا ۲۵ درصد موارد بیماری را شامل میشود. اطلاعاتِ ژنتیکیِ دیانای میتوکندری، در ساخت چندین آنزیم کلیدی در تولید ATP بکار میرود. شایعترین نوع جهش ژنی در بیماری لی مرتبط با میتوکندریها، «جهشِ نقطهای» در نوکلئوتید ۸۹۹۳ در ژن MT-ATP6 است. سایر موارد، شاملِ جهش در ژنهای MTND2، MTND3، MTND5 و MTND6 است. دیانای میتوکندی، همواره از مادر به ارث میرسد (چه در فرزند مذکر و چه مؤنث) و نوعی وراثتِ غیرمندلی است و هرگز از پدر به ارث نمیرسد.
- جهش دیانای هستهای
۷۵ تا ۸۰ درصدموارد بیماری را شامل میشود. دیانای هستهای، بخش اعظمِ ژنوم جانداران را تشکیل میدهد و اگر سندرم لی به دلیل جهش در این ژنها باشد، توارث آن به صورت «اتوزومال مغلوب» است. این جهش، کمپلکس چهارمِ فسفریلاسیون اکسیداتیو و سیتوکروم اکسیداز سی (COX) را مختل میکند و شایعترین نوع آن، جهش در ژنِ «SURF1» است که در بازوی بلند کروموزوم ۹ قرار گرفتهاست. جهشهای ژنی در SURF1 زیرگروههای متفاوتی دارد و در برخی از آنها، علائم بیماری در سنین بالاتری خود را نشان میدهند و روند بیماری در افراد مبتلا، بسیار متغیر است. نوع دیگری از جهش ژنی که در بیماری لی رخ میدهد، جهشی است که عملکردِ پروتئین «پیرووات دِ هیدروژناز» را مختل میکند که یکی از آنزیمهای مهم راهِ گلیکولیز است.
سایر انواع جهش ژنهای هستهای در بیماری لی در این مکانها رخ میدهند:
- کروموزوم ۲: ژنهای BCS1L و NDUFA10
- کروموزوم ۵: ژنهای SDHA، NDUFS4، NDUFAF2 و NDUFA2
- کروموزوم ۸: ژن NDUFAF6
- کروموزوم ۱۰: ژن COX15
- کروموزوم ۱۱: ژنهای NDUFS3، NDUFS8 و FOXRED1
- کروموزوم ۱۲: ژنهای NDUFA9 و NDUFA12
- کروموزوم ۱۹: ژن NDUFS7
بسیاری از این ژنها، کمپلکسِ اولِ فسفریلاسیون اکسیداتیو را تحتِ کنترل دارند.
- بیماری وابسته به کروموزوم X مغلوب
یکی از دلایل دیگر بیماری لی، کمبود «کمپلکس پیرووات دِ هیدروژناز» (PDHC) است که یکی از زیربخشهای آن توسط ژنی به نام «OMIM» که بر روی کروزوم X قرار دارد، کُد میشود. علائم مغزی و عصبی این نوع از بیماری لی، کاملاً مشابه انواع دیگر است؛ اما علائم غیرعصبی (به استثنای اسیدوز لاکتیک) در این نوع از بیماری لی، دیده نمیشود. احتمال ابتلایِ جنین مذکر در این نوع وراث، بیشتر از دختران است؛ چرا که فقط یک نسخهٔ معیوب از کروموزوم X برای ابتلای آنان کافی است، حال آنکه جنین مؤنث برای ابتلا به بیماری، باید هر دو نسخهٔ کروموزوم X معیوب را دریافت دارد.
- سندرم لی در کاناداییهای فرانسویتبار
نوعی از بیماری لی که در ناحیهٔ سگنه-لاک-سن-ژان در مرکز استان کبکِ کانادا شیوع بیشتری دارد، در اثر جهش در ژن «LRPPRC» رخ میدهد که بر روی بازوی کوتاه کروموزوم شماره ۲ واقع است و نخستین بار در سال ۱۹۹۳ میلادی بر روی ۳۴ کودک مبتلا به کمبودِ شدیدِ سیتوکروم اکسیداز سی (COX) کشف شد. این کمبود آنزیمی، در مغز و کبد نزدیک به ۱۰۰ درصد و در فیبروبلاستها و ماهیچههای اسکلتی در حدود ۵۰ درصد بود. بافت قلب و کلیه کمبود COX نداشتند. علائم این نوع از بیماری لی، مشابه سایر انواع است. سنِ شروعِ علائم بهطور میانگین، ۵ ماهگی است و میانگین سنِ مرگ، ۱ سال و ۷ ماهگی است. اختلالهای تحولی خاص، تغییرات خفیف در چهره همچون هایپوپلازی میانهٔ صورت، پُل بینیِ پهن، اسیدوز متابولیک مزمن و هایپوتونی (شُلی عضلانی) در این کودکان دیده میشود. علائم دیگری همچون تاکیپنه، هیپوگلیسمی، لرزش هم وجود دارد و اسیدوز متابولیکِ ناگهانی و شدید، یکی از دلایلِ اصلیِ مرگ است. در جمعیتِ عادیِ مردمِ این ناحیه، ۱ از ۲۳ تا ۱ از ۲۸ نفر، حاملِ ژنِ معیوب هستند و احتمال بروز بیماری در جنین، ۱ از ۲۰۶۳ تا ۱ از ۲۴۷۳ تولدِ زنده است. بر اساس مطالعات ژنتیکیِ انجامیافته، حدس زده میشود که نخستین جهشهای ژنی را، مهاجران اروپایی به این ناحیه از کانادا آورده باشند.
پاتوفیزیولوژی
بخشی از علائم و مشخصات بیماری لی به سببِ ضایعاتِ موضعی در ساقه مغز، عقدههای قاعدهای مغز، مخچه و سایر نواحی مغز است. این ضایعات موضعی به اَشکالِ گوناگون همچون، دِمیلینهشدن، اسفنجیشدن، گلایوز، نکروز و رشد مویرگی است. دِمیلینهشدن، عبارت است از «از دست رفتنِ غلاف میلینِ اطراف آکسون در سلولهای عصبی» که منجر میشود این سلولها نتوانند با یکدیگر ارتباط عصبی داشته باشند. ساقهٔ مغز انسان در اعمال حیاتی اولیه و مهمی چون تنفس، بلع و گردش خون نقش دارد. عقدههای قاعدهای مغز، مخچه در حرکات بدن و تعادل نقش دارند. آسیب به این نواحی، موجب اختلال در عملکردهای مهم آنان میشود. دلیل اسیدوز لاکتیک، تجمع مادهٔ پیرووات به دلیل اختلال در فسفریلاسیون اکسیداتیو است. پیرووات اضافی، دو سرنوشت دارد: یا توسط آنزیم آلانین آمینوترانسفراز به آلانین مبدل میشود؛ یا آنکه توسط آنزیم «لاکتات دِهیدروژناز» به اسید لاکتیک تبدیل میشود. در پایان، هر دوی این محصولاتِ نهایی، در بدن تجمع مییابند.
تشخیص
سندرم لی توسط مجموعهای از یافتههای بالینی، تستهای آزمایشگاهی و ژنتیک تشخیص داده میشود.
یافتههای بالینی
دیستونی، نیستاگموس و اختلالاتِ سیستمِ اتونوم، نشانهای از آسیب به ساقه مغز و عقدههای قاعدهای مغز است. پرمویی و ناشنوایی عصبی هم از علائم دیگر بیماری است.
یافتههای آزمایشگاهی
اسیدوز لاکتیک، اسیدمی و هایپرآلانینمیا (بالا رفتن سطح آلانین خون) و همچنین ارزیابی سطح «اسیدهای ارگانیک ادرار» میتوانند در تشخیص بیماری کمککننده باشند.
تشخیصهای افتراقی
برخی بیماریهای دیگر وجود دارند که علائمشان، شبیه به بیماری لی است و لازم است پیش از تشخیصِ بیماری لی، احتمال وجود این اختلالات، رد شده باشد. این بیماریها عبارتند از: آسفیکسی پریناتال (کمبود اکسیژنِ جنین حوالی تولد)، مسمومیت با منوکسید کربن، مسمومیت با متانول، کمبود ویتامین ب۱، بیماری ویلسون، آنسفالیت و «بیماری عقدههای قاعدهای مغز مرتبط با بیوتین». آسفیکسی پریناتال موجب آسیب دوطرفه به عقدههای قاعدهای و همچنین تالاموس شده و علائمی مشابه سندرم لی ایجاد میکند. اگر هیپربیلیروبینمی نوزادان با نوردرمانی برطرف نشود، بیلیروبین در عقدههای قاعدهای تجمع یافته و احتمال بروز علائمی مشابه با سندرم لی وجود دارد؛ هرچند با ابداع و انجام روش نوردرمانی، دیگر این مسئله شیوع چندانی ندارد.
درمان
رژیم تغذیهای
سندرم لی، یک بیماری بسیار نادر است و در حال حاضر درمان قطعی ندارد. رژیم غذایی پُرچربی و کم قند در فرمی از بیماری که ژن کروموزوم X را درگیر کرده، کمککننده است. اگر بیمار کمبود پیرووات دِهیدروژناز دارد، تجویز تیامین (ویتامین B1) ضرورت مییابد. علائم اسیدوز لاکتیک را میتوان با رژیمهای حاوی بیکربنات سدیم و سیترات سدیم بهبود بخشید. دیکلرو استات در درمان اسیدوز لاکتیک این بیماران مؤثر بوده و تحقیقات بیشتری در این مورد در حالِ انجام است.کوآنزیم کیو ۱۰ در بهبود علائم برخی از بیماران مؤثر بودهاست.
درمان دارویی
هماکنون آزمایشهای بالینی با داروی جدیدی به نام EPI-743 در جریان است.
درمان مبتنی بر جابهجایی میتوکندی
در این روش از میتوکندری فرد دیگری استفاده میشود. در ۲۷ سپتامبر ۲۰۱۶ اولین نوزاد (پسر) با سه والد به دنیا آمد! مادر این پسر حامل ژنهای سندرم لی بود که به دو کودک پیشین این مادر که هر دو مرده بودند٬ انتقال یافته بود. این زن همچنین چهار بار دچار سقط جنین شده بود. این زن به همراه همسر خود به مرکز باروری نیو هوپ در منهتن نیویورک روی آوردند تا نوزادی داشته باشند که از لحاظ ژنتیکی به آنان مربوط باشد، اما حامل ژنهای این بیماری ارثی نباشد. از آنجایی که آمریکا اجازه استفاده از روش سهوالدی را برای مقاصد باروری نمیدهد، پزشک آنها ژانگ در ماه مه برای انجام این کار به مکزیک رفت که به قول او در آن کشور قانونی در این زمینه وجود ندارد.
یک روش دیگر برای حل مشکل این زوج به نام انتقال پیشهستهای (pronuclear transfer) از نظر آنان قابلقبول نبود زیرا انجام آن مستلزم نابودی دو رویان بود.
ازآنجاییکه مادر ژنهای این بیماری را در میتوکندری حمل میکند و در نتیجه DNA معیوب از طرف مادری انتقال مییابد، ژانگ از DNA هستهای تخمک مادر استفاده کرد و به شیوهٔ «انتقال هستهای دوکی»، آن را با میتوکندری بهدستآمده از یک سلول تخمک اهدایی ترکیب کرد. او برای انجام این کار هسته یکی از تخمکهای مادر را خارج کرد و آن را به درون یک تخمک اهدایی که قبلاً هسته آن خارج شده بود، وارد کرد.
تخمک حاصل - حاوی DNA هستهای مادر و DNA میتوکندری از اهداکننده- بعداً با اسپرم پدر بارور شد. ژانگ با این شیوه پنج رویان را به وجود آورد، اما فقط یکی از آنها بهطور طبیعی رشد کرد. این رویان به رحم زن منتقل شد و به تولد پسری انجامید که ظاهراً سالم است.
در آینده میتوان دربارهٔ ایمنی این روش نظر داد.
پیشآگهی
بیماری لی از لحاظ ژنتیکی و اتیولوژی، دلایل متفاوتی دارد که هریک از این انواع، پیشآگهی متفاوتی دارند اما در مجموع، تمامی آنها پیشآگهیِ بدی دارند. شدیدترین فرمِ بیماری که به دلیل فقدان پروتئینهای خاصی است، ظرف چند سال منجر به مرگ میشود. اگر کمبود پروتئینهای مذکور شدید نباشد، پیشآگهی کمی بهتر است و کودک حدود ۷–۶ سال عمر میکند و گاهی بهندرت، به سالهای نوجوانی هم میرسد.
- مشارکتکنندگان ویکیپدیا. «Leigh disease». در دانشنامهٔ ویکیپدیای انگلیسی، بازبینیشده در ۱۴ اوت ۲۰۱۶.
جستارهای وابسته
|
بیماریهای دستگاه عصبی بخصوص CNS
| |||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| التهاب |
|
||||||||||||||||||||||||
|
انسفالوپاتی/ مغز |
|
||||||||||||||||||||||||
| هردو/هرکدام |
|
||||||||||||||||||||||||
| متابولیسم کربوهیدارتها | |
|---|---|
| عمدتاً مرتبط با دستگاه عصبی | |
| میوپاتی میتوکندریال | |
| بدون نظام اولیه | |
| کرومزومی | |
see also پروتئینهای میتوکندریایی | |



