متابولیسم دارو یا در تعریف کلیتر سوختوساز زیستی مواد بیگانه یا متابولیسم زنوبیوتیک تجزیه متابولیکی داروها و برخی سموم توسط موجودات زنده، معمولاً از طریق سیستمهای آنزیمی تخصصی است. این مسیرها شکلی از تبدیل زیستی هستند که در همگی گروههای اصلی موجودات زنده وجود دارد و دارای منشأ باستانی هستند. این واکنشها اغلب برای سمزدایی ترکیبات سمی عمل میکنند (اگرچه در برخی موارد واسطههای متابولیسمی میتوانند اثرات سمی ایجاد کنند). مطالعهٔ متابولیسم داروها را فارماکوکینتیک مینامند.
متابولیسم داروها یکی از جنبههای مهم داروشناسی و پزشکی است. برای مثال، سرعت متابولیسم، مدت و شدت اثر فارماکولوژیک دارو را تعیین میکند. متابولیسم دارو همچنین بر مقاومت چند دارویی در بیماریهای عفونی و شیمیدرمانی سرطان تأثیر میگذارد و عملکرد برخی داروها بهعنوان سوبسترا یا مهارکننده آنزیمهای دخیل در متابولیسم دارویی یکی از دلایل رایج تداخلات دارویی خطرناک است. این مسیرها همچنین در علوم محیطی مهم هستند، زیرا متابولیسم حذف داروها و سموم توسط میکروارگانیسمها تعیین میکند که آیا یک آلاینده در طی زیستپالایی تجزیه میشود یا در محیط باقی میماند. آنزیمهای متابولیسم دارویی، بهویژه گلوتاتیون S-ترانسفرازها نیز در کشاورزی مهم هستند، زیرا ممکن است در برابر آفتکشها و علفکشها مقاومت ایجاد کنند.
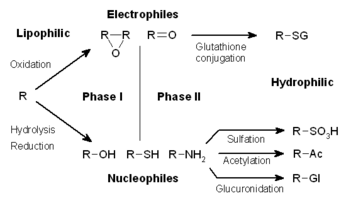
متابولیسم دارو به سه مرحله تقسیم میشود. در فاز I، آنزیمهایی مانند سیتوکروم پی ۴۵۰ اکسیدازها گروههای واکنشی یا قطبی را وارد ترکیبات زیستی بیگانه میکنند. سپس این ترکیبات اصلاح شده در واکنشهای فاز II به ترکیبات قطبی کونژوگه میشوند. این واکنشها توسط آنزیمهای ترانسفراز مانند گلوتاتیون S-ترانسفرازها کاتالیز میشوند. در نهایت، در فاز III، ترکیبات کونژوگه ممکن است بیشتر پردازش شوند، پیش از اینکه توسط انتقالدهندههای جریان، شناسایی و از سلولها پمپ شوند. متابولیسم دارو اغلب ترکیبات چربیدوست را به محصولات آبدوست تبدیل میکند که بهراحتی دفع میشوند.
موانع نفوذپذیری و سمزدایی
ترکیبات دقیقی که یک جاندار در معرض آنها قرار میگیرد تا حد زیادی غیرقابل پیشبینی خواهد بود و ممکن است در طول زمان، بسیار متفاوت باشد. اینها ویژگیهای اصلی استرس سمی زنوبیوتیک هستند. چالش اصلی سیستمهای سمزدایی زنوبیوتیک این است که آنها باید بتوانند تعداد تقریباً نامحدودی از ترکیبات زنوبیوتیک را از مخلوط پیچیدهای از مواد شیمیایی دخیل در متابولیسم طبیعی حذف کنند. راه حلی که برای رفع این مشکل تکامل یافتهاست، ترکیبی هوشمندانه از موانع فیزیکی و سیستمهای آنزیمی با اختصاصیت کم است.
مراحل سمزدایی
متابولیسم زنوبیوتیکها اغلب به سه مرحله تقسیم میشود: اصلاح، کونژوگاسیون و دفع. این واکنشها برای سمزدایی زنوبیوتیکها و حذف آنها از سلولها هماهنگ عمل میکنند.
سموم درونزا
سمزدایی متابولیتهای واکنشی درونزا مانند پراکسیدها و آلدئیدهای واکنشی اغلب توسط سیستمی که در بالا توضیح داده شد قابل دستیابی نیست. این نتیجهٔ این است که این انواع از ترکیبات سلولی طبیعی مشتق شدهاند و معمولاً ویژگیهای قطبی خود را به اشتراک میگذارند. با این حال، از آنجایی که تعداد این ترکیبات کم است، این امکان برای سیستمهای آنزیمی وجود دارد که از تشخیص مولکولی خاص برای شناسایی و حذف آنها استفاده کنند؛ بنابراین شباهت این مولکولها به متابولیتهای مفید به این معنی است که معمولاً آنزیمهای سمزدایی متفاوتی برای متابولیسم هر گروه از سموم درونزا مورد نیاز است. نمونههایی از این سیستمهای سمزدایی خاص عبارتاند از سیستم گلیوکسالاز که برای دفع آلدهید متیلگلیوکسال فعال عمل میکند و سیستمهای آنتیاکسیدانی مختلفی که گونههای فعال اکسیژن را حذف میکنند.
جایگاهها
از نظر کمی، شبکه آندوپلاسمی صاف در سلول کبدی جایگاه اصلی متابولیسم دارو است، اگرچه هر بافتی توانایی متابولیزه کردن داروها را دارد. عواملی که مسئول سهم کبد در متابولیسم دارو هستند عبارتاند از: بزرگ بودن کبد، کبد نخستین عضوی است که توسط مواد شیمیایی جذب شده در روده پرفیوژن میشود، و غلظت بسیار بالایی از بیشترِ سیستمهای آنزیمی متابولیسم دارو نسبت به سایر اندامها وجود دارد. اگر دارویی وارد دستگاه گوارش شود، جایی که از طریق سیاهرگ باب کبدی وارد گردش خون کبدی شود، بهخوبی متابولیزه میشود و گفته میشود که اثر عبور اول را نشان میدهد.
سایر جایگاههای متابولیسم دارو شامل سلولهای بافت پوششی دستگاه گوارش، ریهها، کلیهها و پوست است. این مکانها معمولاً مسئول واکنشهای سمیت موضعی هستند.
عوامل مؤثر بر متابولیسم دارو
مدت و شدت اثر فارماکولوژیک بیشتر داروهای چربیدوست با سرعت متابولیزه شدن آنها به محصولات غیرفعال تعیین میشود. سیستم مونواکسیژناز سیتوکروم پی۴۵۰ مهمترین مسیر در این زمینه است. بهطور کلی، هر چیزی که سرعت متابولیسم (مثلاً القای آنزیم) یک متابولیت فعال دارویی را افزایش دهد، مدت و شدت اثر دارو را کاهش میدهد. عکس آن نیز صادق است (برای مثال، مهار آنزیم). با اینحال، در مواردی که یک آنزیم، مسئول متابولیسم یک داروی جانبی به یک دارو است، القای آنزیم میتواند این تبدیل را تسریع کند و سطح دارو را افزایش دهد و بهطور بالقوه باعث ایجاد سمیت شود.
عوامل مختلف فیزیولوژیکی و پاتولوژیک نیز میتوانند بر متابولیسم دارو تأثیر بگذارند. عوامل فیزیولوژیکی که میتوانند بر متابولیسم دارو تأثیر بگذارند عبارتاند از: سن، تغییرات فردی (مثلاً فارماکوژنتیک)، گردش خون رودهای کبدی، تغذیه، فلور روده یا تفاوتهای جنسی.
بهطور کلی، داروها در انسانها و حیوانات در دورههای جنینی، نوزادی و سالمندی نسبت به بزرگسالان کندتر متابولیزه میشوند. تنوع ژنتیکی (پلیمورفیسم) نیز بخشی از تنوع در اثر داروها به حساب میآید.
آنزیمهای سیستم مونوکسیژناز سیتوکروم پی۴۵۰ نیز میتوانند در افراد مختلف متفاوت باشند و بسته به پیشینهٔ نژادی و قومیتی، کمبود آن در ۱ تا ۳۰ درصد افراد رخ میدهد. دوز، فرکانس، مسیر مصرف، توزیع بافتی و اتصال پروتئین-دارو بر متابولیسم آن تأثیر میگذارد.
عوامل پاتولوژیک نیز میتوانند بر متابولیسم دارو تأثیر بگذارند، از جمله بیماریهای کبد، کلیه یا قلبی.
در روشهای مدلسازی و شبیهسازی سیلیکونی اجازه داده میشود تا متابولیسم دارو در جمعیتهای بیمار مجازی پیش از انجام مطالعات بالینی در افراد پیشبینی شود. این روش میتواند برای شناسایی افراد در معرض خطر بیشتر از واکنشهای نامطلوب استفاده شود.
جستارهای وابسته