سل
| سل | |
|---|---|
| تخصص |
بیماری عفونی (تخصص پزشکی)، پزشکی ریه |
| فراوانی | 0.043—0.045% (سورینام), 0.00033—0.00053% (ایسلند), 0.077—0.079% (اکوادور), -0.99—1.01% (نروژ), -0.00088—0.00112% (فرانسه), 0.0029% (ایالات متحده آمریکا), 0.0028% |
| طبقهبندی و منابع بیرونی | |
| آیسیدی-۱۰ | A15–A19 |
| آیسیدی-۹-سیام | 010–018 |
| اُمیم | ۶۰۷۹۴۸ |
| دادگان بیماریها | 8515 |
| مدلاین پلاس | 000077 ۰۰۰۶۲۴ |
| ئیمدیسین | med/۲۳۲۴ emerg/618 radio/۴۱۱ |
| پیشنت پلاس | سل |
| سمپ | D014376 |
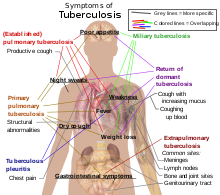
سل یک بیماری عفونی شایع، و در بسیاری از موارد مرگبار است. این بیماری توسط گونههای مختلف مایکوباکتریا، بهطور معمول «مایکوباکتریوم توبرکلوزیس» ایجاد میشود. انتقال باکتری توسط قطرکهای تنفسی از فرد بیمار میباشد. سل بهطور معمول به ششها حمله میکند، اما بر قسمتهای دیگر بدن نیز میتواند تأثیرگذار باشد. وقتی افرادی که عفونت سلی فعال دارند سرفه، عطسه، یا بزاق خود را از طریق هوا منتقل میکنند سل از طریق هوا پخش میشود. اغلب عفونتها بدون علامت و پنهان هستند؛ اما معمولاً از هر ده عفونت نهفته یک عفونت در نهایت پیشرفت کرده و به بیماری فعال تبدیل میشود. اگر سل درمان نشود، بیش از ۵۰٪ از افرادی که به آن آلوده میشوند را به کام مرگ میکشاند.
علائم کلاسیک عفونت سل فعال عبارتند از سرفه مزمن با خلط آغشته به خون، تب، تعریق شبانه، و کاهش وزن. (سل قبلاً به دلیل کاهش وزن افراد به «زوال» مبتلا معروف بود) عفونت اندامهای دیگر باعث طیف وسیعی از علائم میشود. تشخیص سل فعال به رادیولوژی (معمولاً عکس از قفسه سینه با X-ray) و همچنین آزمایشهای میکروسکوپی و کشت میکروبیولوژیک مایعات بدن متکی است. تشخیص سل نهفته متکی بر تست پوستی توبرکولین (TST) و آزمایش خون میباشد. درمان دشوار است و مستلزم آن است که آنتیبیوتیکهای متعددی در یک مدت زمان طولانی استفاده شوند. ارتباطات اجتماعی نیز غربالگری و در صورت لزوم مورد درمان قرار میگیرند. مقاومت در برابر آنتی بیوتیکها یک مشکل رو به رشد در عفونتهای سل مقاوم در برابر داروهای چندگانه (MDR-TB) میباشد. برای جلوگیری از سل، مردم باید برای این بیماری غربالگری و با واکسن bacillus Calmette-Guérin واکسینه شوند.
کارشناسان معتقدند که یک سوم از جمعیت جهان مبتلا به «M. tuberculosis» هستند، و در هر ثانیه یک نفر به این تعداد افزوده میشود. در سال ۲۰۰۷، ۱۳٫۷ میلیون مورد مزمن در سطح جهان فعال بودند. در سال ۲۰۱۰، حدود ۸٫۸ میلیون مورد جدید به وجود آمده و ۱٫۵ میلیون مورد به مرگ انجامید، که عمدتاً در کشورهای در حال توسعه رخ داده است. تعداد مطلق موارد ابتلا به سل از سال ۲۰۰۶ رو به کاهش بودهاست، و موارد جدید از سال ۲۰۰۲ کاهش یافتهاست. سل بهطور یکنواخت در سراسر جهان توزیع نشده است. تست توبرکولین حدود ۸۰٪ از جمعیت حاضر در بسیاری از کشورهای آسیایی و آفریقایی مثبت بوده است، اما تنها تست ۵–۱۰٪ از جمعیت ایالات متحده مثبت بوده است. مردم کشورهای در حال توسعه به دلیل کمبود ایمنی، بیشتر در معرض خطر سل قرار دارند. بهطور معمول، این افراد به دلیل آلوده بودن به HIV و ابتلا به ایدز گرفتار سل میشوند. بیش از ۹۰٪ موارد بیماری و مرگ ناشی از سل در کشورهای در حال توسعه رخ میدهد، کشورهایی که %۷۵ موارد بیماری در آنها به فعالترین گروه سنی به لحاظ اقتصادی (یعنی ۱۵ تا ۵۴ سالگی) تعلق دارد. در این کشورها یک فرد بزرگسال مبتلا به سل بهطور متوسط ۳ الی ۴ ماه قادر به کار کردن نبوده و لذا۲۰تا ۳۰٪ درآمد سالانه خانواده وی از دست میرود. با مرگ چنین فردی بهطور متوسط ۱۵ سال درآمد خانواده بهطور یکجا از بین خواهد رفت. بیماری سل که بزرگترین علت مرگ ناشی از بیماریهای عفونی تکعاملی است (حتی بیشتر از ایدز، مالاریا و سرخک)، دارای مرتبه دهم در بار جهانی بیماریهاست و پیشبینی میشود تا سال ۲۰۲۰ همچنان جایگاه کنونی خود را حفظ کند یا تا رتبه هفتم بالا رود.
این بیماری در قدیم به نام تب لازم و هماکنون در مناطقی با نام توبرکلوزیس شناخته میشود.
این بیماری در 51 درصد از انسان ها قابل درمان است .
علائم و نشانهها
حدود ۵–۱۰٪ از افرادی که HIV ندارند، اما آلوده به سل هستند در طول عمر خود دچار بیماری فعال میشوند. در مقابل، ۳۰٪ از افرادی که آلوده به HIV و سل هستند دچار بیماری فعال میگردند. سل میتواند هر قسمتی از بدن را آلوده کند، اما معمولاً در ریهها رخ میدهد (شناختهشده به عنوان سل ریوی). سل خارج ریوی زمانی رخ میدهد که سل به خارج از ریهها نفوذ میکند. سل خارج ریوی همچنین میتواند همزمان با سل ریوی وجود داشته باشد. علائم و نشانههای عمومی عبارتند از تب، لرز، تعریق شبانه، از دست دادن اشتها، کاهش وزن، و خستگی مفرط. همچنین پدیده انگشت چماقی قابل توجهی نیز میتواند رخ دهد.
ریوی
اگر یک عفونت سل فعال شود، در حدود ۹۰٪ از مردم در ریهها بروز میکند. علائم میتواند شامل درد قفسه سینه و سرفههای طولانی باشد که تولید خلط میکنند. در حدود ۲۵٪ از افراد هیچ علائمی ندارند (یعنی آنها «بدون علامت» باقی میمانند). گاهی اوقات، افراد دچار سرفههای خونین در مقادیر کم میشوند. در موارد نادر، عفونت میتواند به تضعیف شریان ریوی بینجامد که منجر به خونریزی شدید به نام آنوریسم راسموسن میشود. سل میتواند تبدیل به یک بیماری مزمن شده و باعث زخمهای گسترده در نرمه فوقانی ریهها شود. قسمت فوقانی ریهها بیشتر تحت تأثیر قرار میگریند. دلیل آن بهطور کامل روشن نیست. شاید قسمت فوقانی ریهها به دلیل جریان هوای بهتر یا خروجی ضعیف غدد لنفاوی بیشتر تحت تأثیر قرار میگیرند.
خارج ریوی
در ۱۵–۲۰٪ از موارد فعال، عفونت به خارج از اندامهای تنفسی گسترش مییابد که باعث بروز انواع دیگر سل میشود به سلی که خارج از اندامهای تنفسی رخ میدهد، «سل خارج ریوی» گفته میشود. سل خارج ریوی بهطور معمول در افرادی که دچار نقص سیستم ایمنی هستند و کودکان رخ میدهد. سل خارج ریوی در بیش از ۵۰٪ از افرادی که HIV دارند دیده میشود. مکانهای عفونت قابل توجه خارج ریوی عبارتند از: شش شامه (در پلورزی (آماس شامه ریه) سلی)، سیستم عصبی مرکزی (در مننژیت سلی)، و سیستم لنفاوی (در سل غدد لنفاوی گردن). از میان مکانهای دیگر سل خارج ریوی در دستگاه ادراری تناسلی (در سل ادراری تناسلی) و در استخوانها و مفاصل (در سل ستون فقرات) نیز اتفاق میافتد. هنگامی که این بیماری در استخوان هم گسترش مییابد، آن را به عنوان «سل استخوانی» نیز میشناسند، که نوعی از استئومیلیت (کورک استخوانی) میباشد. یک نوع بالقوه جدیتر و شایع سل، سل «منتشر» نام دارد که معمولاً به عنوان سل ارزنی یا میلیاری و منتشر شناخته شده است. سل ارزنی در حدود ۱۰٪ از موارد سل خارج ریوی را تشکیل میدهد.
علل
مایکوباکتری
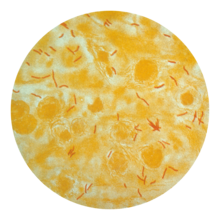
علت اصلی سل «مایکوباکتریوم توبرکلوزیس»، یک باسیل بی حرکت هوازی کوچک است. بسیاری از ویژگیهای بالینی منحصربهفرد این پاتوژن به دلیل محتوای چربی بالای آن ایجاد میشود. این باسیل هر ۱۶ –۲۰ ساعت یک بار تقسیم میشود. سرعت آن در مقایسه با دیگر باکتریها که معمولاً در کمتر از یک ساعت تقسیم میشوند آهسته است.غشای بیرونی میکوباکتریا از دولایه لیپیدی تشکیل شدهاست. اگر یک رنگ آمیزی گرم انجام شود، MTB یا رنگ بسیار کم «گرم مثبت» دارد یا اصلاً رنگی به خود نمیگیرد چرا که دیواره سلولی آن دارای محتوای چربی و اسید مایکولیک بالا میباشد. MTB میتواند در برابر مواد ضد عفونیکننده ضعیف مقاومت کند و در یک شرایط خشک هفتهها زنده بماند. در طبیعت، باکتری تنها میتواند در داخل سلول یک ارگانیسم میزبان رشد کند، اما «M. tuberculosis» میتواند در آزمایشگاه کشت شود.
با استفاده از رنگهای بافتی بر روی نمونههای خلط به دست آمده از سینه، دانشمندان میتوانند MTB را در زیر یک میکروسکوپ معمولی (نوری) تشخیص دهند. MTB رنگهای خاصی را حتی بعد از واکنش با محلول اسیدی حفظ میکند، بنابراین به عنوان باسیل اسید-فاست (مقاوم در برابر رنگ بری اسید) (AFB) طبقهبندی شده است. دو تکنیک رنگآمیزی اسید فاست شایعتر هستند: رنگ آمیزی Ziehl–Neelsen، که AFBها را به رنگ قرمز روشن در میآورد که به وضوح در برابر یک پسزمینه آبی رنگ دیده میشوند، و رنگ آمیزی auramine-rhodamine و پس از آن میکروسکوپ فلورسانس.
مجموعه «M. tuberculosis»(MTBC) شامل چهار میکوباکتری سلزای دیگر میشود: “M. bovis,” “M. africanum,” “M. canetti,” و “M. microti”. «M. africanum» شایع نیست، اما علت قابل توجه ایجاد سل در بخشهایی از آفریقا میباشد. «M. bovis» یک علت شایع سل بود، اما با ظهور شیر پاستوریزه تا حد زیادی این میکوباکتریوم را به عنوان یک مشکل بهداشت عمومی در کشورهای توسعهیافته از بین برد. «M. canetti» نادر است و به نظر میرسد به شاخ آفریقا محدود باشد، اگر چه چند مورد در مهاجران آفریقایی دیده شده است. «M. microti» نیز نادر بوده و اغلب در افراد دارای نقص ایمنی دیده میشود، اما این پاتوژن میتوانست شایعتر از آن باشد که ما فکر میکنیم.
دیگر میکوباکتریهای بیماریزای شناخته شده عبارتند از “M. leprae,” “M. avium,” و “M. kansasii”. دو گونه آخر به عنوان «میکوباکتریهای غیر سلی» (NTM) طبقهبندی شدهاند. NTM باعث ایجاد سل یا جذام نمیشود، اما آنها منجر به بیماریهای ریوی میشوند که شبیه سل است.
عوامل خطرساز
عوامل متعددی مردم را در ابتلا به عفونت سل مستعدتر مینمایند. مهمترین عامل خطرساز در سراسر جهان HIV است؛ ۱۳٪ درصد از تمام موارد ابتلا به سل آلوده به ویروس HIV هستند. این مشکل در کشورهای جنوب صحرای آفریقا، که در آن نرخ HIV بالاست شایع است.
سل به ازدحام بیش از حد و تغذیه نامناسب بسیار مرتبط است. این ارتباط باعث میشود سل یکی از بیماریهای فقر اصلی باشد. این دسته از افراد در معرض خطر بالایی برای عفونت سل قرار دارند: افرادی که مواد مخدر ممنوع تزریق میکنند، ساکنان و کارگران و کارمندان مکانهایی که در آن افراد آسیبپذیر تجمع میکنند (به عنوان مثال، زندانها و پناهگاههای مخصوص بیخانمانها)، افرادی که فقیر هستند و به مراقبتهای پزشکی مناسب دسترسی ندارند، اقلیتهای قومی با خطر بالا، بچهها در تماس نزدیک با افراد با خطر بالا، و ارائهدهندگان مراقبتهای بهداشتی که در خدمت این افراد میباشد.
بیماری ریوی مزمن، یکی دیگر از عوامل خطر ساز قابل توجه است. بیماری سیلیکوز خطر را حدوداً ۳۰ برابر میکند. افرادی که سیگار میکشند نسبت به غیرسیگاریها تقریباً دو برابر در معرض خطر ابتلا به سل هستند.
بیماریهای دیگر نیز میتوانند خطر ابتلا به سل را افزایش دهند، از جمله اعتیاد به الکل و دیابت قندی (خطر را سه برابر میکند). برخی داروها، مانند کورتیکواستروئیدها و اینفیلیکسیماب (یک آنتی بادی مونوکلونال ضد αTNF)، به خصوص در جوامع توسعه یافته از عوامل خطرساز بسیار مهم هستند. همچنین، یک استعداد ژنتیکی نیز وجود دارد، اما دانشمندان مشخص نکردهاند که چقدر مهم است.
مکانیسم
انتقال
هنگامی که افراد مبتلا به سل فعال آواز بخوانند، سرفه، عطسه، صحبت یا تف کند، ذرات عفونی معلق در هوا (بیماری هوابرد) به قطر ۰٫۵ تا ۵ میکرومتر را پخش میکنند. تنها یک عطسه میتواند تا ۴۰٬۰۰۰ قطره را منتشر کند. هر ذره میتواند بیماری را منتقل کند زیرا دوز عفونی سل بسیار پایین است. (کسی که کمتر از ۱۰ باکتری را استنشاق کند میتواند آلوده شود).
مردمی که در تماسهای طولانی مدت، مکرر یا نزدیک با افراد مبتلا به سل هستند در معرض خطر آلوده شدن به عفونت، با نرخ عفونت حدود ۲۲ درصد میباشند. یک فرد مبتلا به سل فعال، اما درمان نشده میتواند ۱۰–۱۵ نفر (یا بیشتر) را در هر سال آلوده کند. بهطور معمول، تنها افراد دارای سل فعال این بیماری را انتقال میدهند. تصور نمیشود که افراد مبتلا به عفونت نهفته مسری باشند. احتمال انتقال از فردی به فرد دیگر به عوامل متعددی بستگی دارد. این عوامل عبارتند از تعداد قطرات عفونی که حامل منتشر میکند، کارآمدی تهویه محیط زیست افراد، مدت زمان در معرض قرار گرفتن، میزان واگیردار بودن گونه «M. tuberculosis»، و سطح ایمنی در فرد غیرآلوده. برای جلوگیری از آبشار شیوع فرد به فرد، افراد مبتلا به سل فعال («آشکار») را جدا میکنند و آنها را تحت رژیمهای داروی ضد سل قرار میدهند. پس از حدود دو هفته درمان مؤثر، بهطور کلی افراد مبتلا به عفونت فعال غیر مقاوم برای دیگران مسری نخواهند بود. اگر کسی آلوده شود، بهطور معمول سه تا چهار هفته طول میکشد تا شخص به تازگی آلودهشده به اندازه کافی برای انتقال بیماری به دیگران مسری شود.
بیماریزایی
در حدود ۹۰٪ درصد از افرادی که مبتلا به «M. tuberculosis» هستند عفونت سل نهفته بدون علامت دارند (که گاهی اوقات LTBI نامیده میشود). این افراد در طول عمر خود تنها ۱۰٪ شانس پیشرفت عفونت نهفته به بیماری سل فعال آشکار را دارند. برای افراد مبتلا به HIV، خطر اینکه آنها به سل فعال مبتلا شوند به نزدیک ۱۰٪ در سال میرسد. اگر درمان مؤثر داده نشود، میزان مرگ و میر در موارد سل فعال تا ۶۶٪ میباشد.
عفونت سل وقتی که میکوباکتریها به حبابچههای ریوی میرسد شروع میشود، جایی که آنها به endosomes از ماکروفاژهای آلوئولی حمله کرده و در داخل آن تکثیر میشوند. محل اولیه عفونت در ریهها، معروف به «کانون گان»، یا در قسمت فوقانی لوب تحتانی، یا در قسمت تحتانی لوب فوقانی واقع شده است. سل ریهها میتواند از طریق عفونت از جریان خون نیز ایجاد شود که به عنوان کانون سیمون شناخته شده است. یک عفونت کانون سیمون بهطور معمول در بالای ریه دیده میشود. این انتقال خونی میتواند بیماری را به محلهای دورتر از جمله غدد لنفاوی محیطی، کلیهها، مغز و استخوانها نیز گسترش دهد. سل بر تمام قسمتهای بدن تأثیر میگذارد، هر چند به دلایل نامعلوم به ندرت قلب، عضلات اسکلتی، لوزالمعده، یا تیروئید را تحت تأثیر قرار میدهد.
سل به عنوان یکی از بیماریهای التهابی گرانولومــاتوز دستهبندی میشود. ماکروفاژها، T لنفوسیتها، B لنفوسیتها، و فیبروبلاستها از جمله سلولهایی هستند که جمع میشوند تا گرانولومها را تشکیل دهند. لنفوسیتها ماکروفاژهای آلوده را احاطه میکنند. گرانولوم از انتشار میکوباکتریها جلوگیری کرده و یک محیط محلی را برای تعامل سلولهای سیستم ایمنی بدن فراهم مینماید. باکتریها در داخل گرانولوم میتوانند ساکت بمانند که منجر به عفونت نهفته میشود. یکی دیگر از ویژگیهای گرانولومها توسعه مرگ سلولی غیرطبیعی (نکروز) در مرکز برآمدگیها است. برای چشم غیرمسلح، این نکروز، بافتی نرم، شبیه پنیر سفید دارد و نکروز پنیری نامیده میشوند.
باکتریهای سل میتوانند از یک منطقه آسیبدیده بافت وارد جریان خون شود. آنها میتوانند در سراسر بدن گسترش یافته و کانونهای متعدد عفونت را ایجاد کنند که مانند برآمدگیهای کوچک سفید در بافتها دیده میشوند. این نوع شدید از بیماری سل سل ارزنی نامیده میشود. این شکل از سل بیشتر در کودکان و افراد مبتلا به HIV شایع است. افراد مبتلا به سل منتشر، حتی با درمان هم میزان مرگ و میر بالایی دارند (حدود ۳۰٪).
در بسیاری از مردم، عفونت ظهور و افول دارد. تخریب و نکروز بافت اغلب با بهبود و فیبروز متعادل میشود. بافت متأثر، با جای زخم و حفرههای پُرشده با مواد نکروز پنیری جایگزین میشود. در بیماری فعال، برخی از این حفرهها به راههای هوایی نایژهها پیوسته و این مواد میتوانند با سرفه کردن بیرون بریزند. این مواد حاوی باکتری زنده هستند و میتوانند عفونت را پخش کنند. درمان با آنتی بیوتیکهای مناسب، باکتریها را میکشد و امکان بهبودی را فراهم میکند. هنگامی که بیماری درمان شد، مناطق آسیبدیده توسط بافتهای همبند جای زخم جایگزین میشوند.
تشخیص
سل فعال
تشخیص سل فعال صرفاً بر اساس علائم و نشانهها دشوار است. همچنین تشخیص بیماری در افرادی که دچار دپرسیون ایمنی هستند نیز مشکل است. با این حال، افرادی که دارای علائم بیماری ریوی یا علائم مزاجی هستند که بیش از دو هفته ادامه مییابند ممکن است سل داشته باشند. یک عکس از قفسه سینه با پرتو ایکس و چند کشت خلط برای باسیلهای اسید فاست بهطور معمول بخشی از ارزیابی اولیه میباشند. آزمونهای اینترفرون گاما ترشحشده (IGRAها) و آزمونهای پوستی توبرکولین در جوامع در حال توسعه مفید نیستند. IGRAها در افراد مبتلا به HIV نیز محدودیتهای مشابهی دارند.
یک تشخیص قطعی سل زمانی انجام میشود که «M. tuberculosis» در یک نمونه بالینی شناسایی شود (برای مثال، خلط چرک، یا یک بیوپسی از بافت). با این حال، با توجه به سرعت دو برابر شدن نزدیک به ۲۰ ساعت (در مقایسه با ۲۰ دقیقه برای e.Coli)، میتواند دو تا شش هفته برای نتیجه کشت خون یا خلط طول بکشد. از این رو، درمان اغلب قبل از تأیید کشتها آغاز میشود.
آزمونهای تقویت اسید نوکلئیک و آزمایش آدنوزین آمیناز میتوانند سل را به سرعت تشخیص دهند. با این حال، این آزمایشها بهطور مداوم توصیه نمیشوند چرا که آنها به ندرت چگونگی درمان یک فرد را تغییر میدهند. آزمایش خون برای تشخیص آنتیبادیها دقیق یا حساس نیستند، بنابراین توصیه نمیشوند.
سل نهفته
تست پوستی توبرکولین مانتو اغلب برای غربالگری افراد در معرض خطر بالای بیماری سل استفاده میشود. این تست میتواند در افراد مبتلا به سارکوئیدوز، لنفوم هوچکین، و سوء تغذیه به صورت کاذب منفی باشد. مهمتر از همه، این تست میتواند در افرادی که سل فعال دارند به صورت کاذب منفی باشد.سنجش اینترفرون گامای آزاد (IGRAها) در یک نمونه خون برای افرادی که تست مانتو مثبت دارند توصیه میشود. IGRAها تحت تأثیر ایمنسازی یا اکثر میکوباکتریهای زیستمحیطی قرار نمیگیرند، بنابراین آنها نتایج مثبت کاذب کمتری ارائه میکنند. با این حال آنها تحت تأثیر «M. szulgai»، «M. marinum» و «M. kansasii» قرار میگیرند. IGRAها زمانی که همراه با تست پوستی استفاده میشوند میتوانند حساسیت بیشتری داشته باشند. اما وقتی IGRAها به تنهایی استفاده میشوند میتوانند حساسیت کمتری نسبت به تست پوستی داشته باشند.
پیشگیری
تلاش برای جلوگیری و کنترل سل بر واکسیناسیون نوزادان و تشخیص و درمان مناسب موارد فعال متکی میباشد.سازمان بهداشت جهانی (WHO) موفقیتهایی را در رژیمهای درمانی بهبودیافته به دست آورده است. کاهش اندکی در تعداد موارد دیده شده است.
واکسنها
تا سال ۲۰۱۱، تنها واکسن سل موجود (Bacillus Calmette-Guérin یا ب.ث. ژ) میباشد. BCG در برابر بیماریهای منتشرشده در دوران کودکی مؤثر است اما حفاظت متناقضی را در برابر ابتلا به سل ریوی ایجاد میکند. با این حال، این گستردهترین واکسن مورد استفاده در سراسر جهان است، که بیش از ۹۰٪ از همه کودکان را واکسینه میکند. با این حال، ایمنی ایجادشده توسط آن بعد از حدود ده سال کاهش مییابد. سل در اکثر نقاط کانادا، بریتانیا، و ایالات متحده شایع نیست، بنابراین BCG فقط برای افرادی که در معرض خطر بالا قرار دارند استفاده میشود. یکی از دلایل عدم استفاده از واکسن این است که باعث میشود تست پوستی توبرکولین مثبت کاذب شود که این آزمون را برای غربالگری این بیماری بیفایده مینماید. واکسنهای جدید در دست تهیه هستند.
بهداشت عمومی
سازمان جهانی بهداشت در سال ۱۹۹۳ سل را «وضعیت اضطراری برای بهداشت جهانی» اعلام کرد. در سال ۲۰۰۶، مشارکت توقف سل، طرح جهانی برای متوقف کردن سل را مطرح کرد که قرار است تا سال ۲۰۱۵ جان ۱۴ میلیون نفر را حفظ کند. تعدادی از اهداف تعیینشده به احتمال زیاد تا سال ۲۰۱۵ حاصل نمیشوند، این امر بیشتر به دلیل افزایش سل مرتبط با HIV و ظهور سل مقاوم در برابر چند دارو (MDR-TB) میباشد. سیستم طبقهبندی سل که جامعه بیماریهای صدری آمریکا آن را تهیه کرده است در برنامههای بهداشت عمومی استفاده میشود.
مدیریت
درمان سل از آنتیبیوتیکها برای از بین بردن باکتریها استفاده میکند. درمان مؤثر سل مشکل است که به دلیل ساختار غیرمعمول و ترکیب شیمیایی دیواره سلولی میکوباکتریومی میباشد. دیواره سلولی داروها را بیرون نگه میدارد و باعث میشود که بسیاری از آنتیبیوتیکها بیاثر شوند. دو آنتیبیوتیکی که بیشترین استفاده را دارند ایزونیازید و ریفامپیسین هستند و درمان میتواند ماهها ادامه یابد. در درمان سل نهفته معمولاً تنها از یک آنتیبیوتیک استفاده میشود. بیماری سل فعال، به منظور کاهش خطر ایجاد مقاومت در برابر آنتیبیوتیک در باکتری، با ترکیبی از چند آنتیبیوتیک بهتر درمان میشود. افراد مبتلا به عفونت نهفته نیز درمان میشوند تا از ابتلای آنها به بیماری سل فعال در آینده جلوگیری شود. WHO درمان با مشاهده مستقیم را توصیه میکند. در این روش درمانی، ارائهدهنده مراقبتهای بهداشتی مصرف دارو توسط فرد را مشاهده مینماید. هدف کاهش تعداد افرادی است که آنتیبیوتیکها را بهطور مناسب مصرف نمیکنند. با این حال، شواهد برای حمایت از درمان با مشاهده مستقیم ضعیف است. روشهایی که به مردم یادآوری میکند که درمان بسیار مهم است مؤثر میباشند.
شروع جدید
در سال ۲۰۱۰، درمان توصیهشده برای سل ریوی تازه بروز کرده، ترکیبی از آنتیبیوتیکها به مدت شش ماه میباشد. برای دو ماه اول، ریفامپیسین، ایزونیازید، پیرازینامید و اتامبوتول تجویز شود. در چهار ماه بعد، تنها ریفامپیسین و ایزونیازید تجویز شود. در صورتی که مقاومت به ایزونیازید بالا باشد، میتوان به جای آن از اتامبوتول در چهار ماه پایانی استفاده کرد.
بیماری عودکننده
اگر سل عود کند، قبل از شروع درمان برای تعیین آنتیبیوتیکهایی که به آن حساس است آزمایش انجام دهید. اگر سل مقاوم به چند دارو (MDR-TB) تشخیص داده شود، درمان با حداقل چهار آنتیبیوتیک مؤثر برای ۱۸–۲۴ ماه توصیه میشود.
مقاومت به دارو
مقاومت اولیه هنگامی رخ میدهد که فرد به یک گونه مقاوم سل مبتلا میشود. فرد مبتلا به سل کاملاً حساس (مستعد) ممکن است در طول درمان دچار مقاومت ثانویه (اکتسابی) شود. یک فرد در صورتی که از رژیم تجویزشده بهطور مناسب پیروی نکند (عدم تطابق)، یا اگر از داروهایی با کیفیت پایین استفاده کند، ممکن است به دلیل درمان نامناسب دچار مقاومت ثانویه شود. سل مقاوم در برابر دارو، یک مسئله جدی در بهداشت عمومی بسیاری از کشورهای در حال توسعه است. درمان سل مقاوم در برابر دارو طولانیتر است و به داروهای گرانتر نیاز دارد. MDR-TB به عنوان مقاومت در برابر دو داروی مؤثر رده اول سل: ریفامپیسین و ایزونیازید، تعریف شده است. سل بسیار مقاوم در برابر دارو در برابر سه یا بیشتر از سه مورد از شش کلاس داروهای رده دوم مقاوم است.سل کاملاً مقاوم در برابر دارو نسبت به تمام داروهایی که در حال حاضر استفاده میشود مقاوم است. سل کاملاً مقاوم در برابر دارو برای اولین بار در سال ۲۰۰۳ در ایتالیا مشاهده شد اما از آن به بعد تا سال ۲۰۱۲ بهطور گسترده گزارش نشده است. موارد multidrug-resistant TB) MDR-TB) در سال ۲۰۱۳ حدود ۳٫۵٪ در موارد جدید و ۲۰٫۵٪در موارد قدیمی و قبلی بودهاست. پیشبینی میشد حدود۳۰۰/۰۰۰ مورد MDR-TB در سال ۲۰۱۳ وجود داشته باشند که ۱۳۶۰۰۰ نفر (در حدود ۴۵٪ موارد) شناسایی و گزارش شدند.
پیش شناخت
پیشرفت عفونت سل به بیماری سل آشکار زمانی رخ میدهد که باسیل بر دفاعهای سیستم ایمنی غلبه و شروع به تکثیر کند. در بیماری سل اولیه (حدود ۱–۵٪ از موارد)، این پیشرفت به سرعت پس از عفونت اولیه رخ میدهد. با این حال، در اکثر موارد، یک عفونت نهفته بدون هیچ نشانه آشکاری رخ میدهد. این باسیلهای خفته باعث ایجاد سل فعال در ۵–۱۰٪ از این موارد نهفته میشوند و اغلب این امر سالها پس از عفونت اتفاق میافتد.
خطر فعال شدن مجدد با سرکوب سیستم ایمنی افزایش مییابد، مانند آنچه که از آلودگی به HIV ناشی میشود. در افراد مبتلا به «M. tuberculosis» و HIV، خطر فعالشدن مجدد به ۱۰٪ در سال افزایش مییابد. مطالعاتی که از طرحهای DNA نژادهای «M. tuberculosis» استفاده میکنند، نشان میدهند که عفونت مجدد باعث عود سل بیشتر از آنچه قبلاً تصور میشد میشود. عفونت مجدد ممکن است موجب بیش از ۵۰٪ از موارد فعال شده مجدد در مناطقی که در آن سل شایع است بشود. احتمال مرگ و میر ناشی از سل در حدود ۴٪ در سال ۲۰۰۸ بود، که کمتر از ۸٪ در سال ۱۹۹۵ است.
شیوع
حدود یک سوم از جمعیت جهان با «M. tuberculosis» آلوده شده است. در هر ثانیه یک عفونت جدید در مقیاس جهانی رخ میدهد. با این حال، بسیاری از عفونتها به «M. tuberculosis» منجر به بیماریهای سل نمیشود، و ۹۰–۹۵٪ از عفونتها بدون علامت باقی میمانند. در سال ۲۰۰۷، حدود ۱۳٫۷ میلیون مورد مزمن فعال وجود داشت. در سال ۲۰۱۰، ۸٫۸ میلیون مورد جدید سل، و ۱٫۴۵ میلیون مرگ و میر شناسایی شد، که بیشتر اینها در کشورهای در حال توسعه اتفاق میافتد. از این ۱٫۴۵ میلیون مرگ و میر، در حدود ۰٫۳۵ میلیون نفر در افراد آلوده به HIV رخ داد.
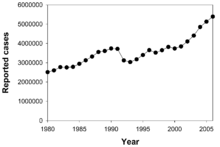
سل دومین علت شایع مرگ ناشی از بیماریهای عفونی (پس از مرگ به علت HIV/AIDS) است. تعداد مطلق موارد ابتلا به سل («شیوع») از سال ۲۰۰۵ رو به کاهش بوده است. موارد جدید سل («بروز») از سال ۲۰۰۲ کاهش یافته است. چین به خصوص پیشرفت چشمگیری داشته است. چین میزان مرگ و میر ناشی از سل خود را بین سالهای ۱۹۹۰ و ۲۰۱۰ حدود ۸۰٪ کاهش داده است. سل در کشورهای در حال توسعه شایعتر است. حدود ۸۰٪ از جمعیت بسیاری از کشورهای آسیایی و آفریقایی در آزمون توبرکولین تست مثبت داشتهاند اما تنها ۵–۱۰٪ از جمعیت ایالات متحده آزمون مثبت داشتهاند. کارشناسان امیدوار بودند که سل را بهطور کامل کنترل کنند. با این حال، عوامل متعددی کنترل کامل سل را بعید میکند. تهیه یک واکسن مؤثر دشوار بوده است. تشخیص بیماری گران است و زمان زیادی میبرد. درمان چندین ماه طول میکشد. افراد مبتلا به HIV بیشتری گرفتار سل میشوند. سل مقاوم در برابر دارو در دهه ۸۰ مشاهده شد.
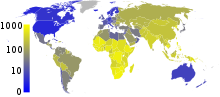
در سال ۲۰۰۷، کشور دارای بیشترین میزان شیوع تخمینی سل، سوازیلند، با ۱٬۲۰۰ مورد در هر ۱۰۰٬۰۰۰ نفر بود. هند بیشترین شیوع در کل را با ۲٫۰ میلیون مورد جدید داشت. در کشورهای توسعهیافته، سل کمتر شایع است و بهطور عمده در مناطق برونشهری یافت میشود. در سال ۲۰۱۰، نرخ TB در هر ۱۰۰٬۰۰۰ نفر در مناطق مختلف جهان بدین شرح بود: در سطح جهانی ۱۷۸، آفریقا ۳۳۲، آمریکا ۳۶، شرق مدیترانه ۱۷۳، اروپا ۶۳، جنوب شرق آسیا ۲۷۸، و غرب اقیانوس آرام ۱۳۹. در کانادا و استرالیا، سل در میان مردم بومی به ویژه در مناطق دور افتاده بسیار رایج است. در ایالات متحده، مرگ و میر ناشی از سل سکنه بومی پنج برابر بیشتر است.
شیوع سل در سنین مختلف متفاوت است. در آفریقا، سل بهطور عمده افراد بین ۱۲ و ۱۸ سال و نوجوانان را تحت تأثیر قرار میدهد. با این حال، در کشورهایی که در آن نرخ بروز سل بهطور چشمگیری کاهش یافته است (مانند ایالات متحده)، سل عمدتاً بیماری افراد پیر و افراد دارای سیستم ایمنی در معرض خطر است. میزان بروز سل در مردان بیشتر از زنان است. در سال ۲۰۱۳ حدود ۵۱۰۰۰۰ زن در نتیجه سل از بین رفتهاند و حدود ۱۸۰۰۰۰ نفر از آنان همزمان آلودگی به HIV داشتهاند. در سال ۲۰۰۷، ۱۳٫۷ میلیون مورد مزمن سل در سطح جهان فعال بودند. در سال ۲۰۱۰، حدود ۸٫۸ میلیون مورد جدید به وجود آمده است. با حدود ۱٫۵ میلیون مرگ. در سال ۲۰۱۳، ۹ میلیون مورد مزمن در سطح جهان فعال بودند با ۱٫۵ میلیون مرگ (۱٫۱ میلیون بدون آلودگی به HIV و ۳۶۰/۰۰۰ نفر با آلودگی بهHIV) از تمام موارد موجود ۵۶٪ موارد در جنوب شرق آسیا و غرب اقیانوس کبیر بودهاند و ۳۶۰/۰۰۰ نفر آلودگی همزمان سل و HIV داشتهاند. بین سالهای ۲۰۰۰ تا ۲۰۱۳، ۳۷ میلیون تشخیص و درمان مؤثر سل انجام شده است. در سرتاسر جهان *میزان بروز سل بین سالهای ۲۰۰۰ تا ۲۰۱۳ حدود ۱٫۵٪ در هر سال کاهش داشته است. در همین بازه زمانی *میزان شیوع سل ۴۱٪ کاهش داشته است. بین سالهای ۱۹۹۰تا ۲۰۱۳ میزان مرگ و میر سل حدود ۴۵٪ کاهش داشته است. میزان درمان موفقیتآمیز در سال ۲۰۱۳ حدود ۸۶٪ موارد کشفشده بود. هدف جهان تا سال ۲۰۳۵ کاهش ۹۵٪ مرگ و میرهای ناشی از سل و کاهش ۹۰٪ بروز موارد جدید است.
تاریخچه
سل از دوران باستان همراه انسان بوده است. قدیمیترین تشخیص بدون ابهام «M. tuberculosis» شامل شواهد این بیماری در بقایای گاومیش کوهاندار آمریکایی است که به ۱۷٬۰۰۰ سال پیش باز میگردد. با این حال، مشخص نیست که آیا سل در گاومیش به وجود آمده و پس از آن به انسان منتقل شدهاست یا اینکه از یک جد مشترک انشعاب یافته است. دانشمندان زمانی اعتقاد داشتند که انسان MTBC را از حیوانات هنگام اهلی کردن آنها گرفته است. با این حال، ژنهای مجموعه «M. tuberculosis» (MTBC) در انسان با MTBC در حیوانات مقایسه شدهاند و ثابت شده است که این تئوری نادرست است. هر دو گونه باکتری سل یک جد مشترک دارند که میتوانسته است انسان را در اوایل انقلاب نوسنگی آلوده کرده باشد. باقیماندههای اسکلتی نشان میدهد که انسانهای ماقبل تاریخ (۴۰۰۰ سال قبل از میلاد مسیح) سل داشتهاند. پژوهشگران پوسیدگی مسلول را در ستون فقرات مومیایی مصری یافتهاند که به ۳۰۰۰–۲۴۰۰ سال قبل از میلاد بازمیگردد. «Phthisis» یک کلمه یونانی به معنی «مصرف» است که اصطلاح قدیمی برای بیماری سل ریوی میباشد. در حدود ۴۶۰ سال قبل از میلاد، بقراط سل ریوی را به عنوان گستردهترین بیماری در آن زمان شناسایی کرد. افراد مبتلا به سل ریوی تب و سرفه خونین داشتند. سل ریوی تقریباً همیشه کشنده بود. مطالعات ژنتیکی نشان میدهد که سل از حدود سال ۱۰۰ میلادی در میان آمریکاییها وجود داشته است.
قبل از انقلاب صنعتی، فرهنگ عامه اغلب سل را با خون آشامها مرتبط میدانسته است. هنگامی که یکی از اعضای خانواده به دلیل سل فوت میکرد، دیگر اعضای آلوده، سلامت خود را به آرامی از دست میدادند. مردم بر این باور بودند که فرد اصلی مبتلا به سل زندگی را از دیگر اعضای خانواده میربوده است.
نوع ریوی مرتبط با برآمدگیها به عنوان یک آسیبشناسی توسط دکتر ریچارد مورتون در سال ۱۶۸۹ تعیین شد. با این حال، سل انواع مختلفی از علائم را داراست، از این رو، سل تا دهه ۲۰ قرن نوزدهم به عنوان یک بیماری واحد شناسایی نشده بود. این بیماری در سال ۱۸۳۹ توسط جی.ال. شوئن سل نامیده شد. طی سالهای ۱۸۳۸–۱۸۴۵، دکتر جان کروگان (John Croghan)، صاحب غار ماموت، افراد مبتلا به سل را به داخل غار میبرد به این امید که این بیماری را با درجه حرارت ثابت و خلوص هوای غار درمان کند: آنها ظرف یک سال درگذشتند. هرمان برمر (Hermann Brehmer) اولین آسایشگاه سل را در سال ۱۸۵۹ در Sokołowsko، لهستان باز کرد.
باسیلی که باعث بیماری سل میشود، «میکوباکتریوم توبرکلوسیس»، در ۲۴ مارس ۱۸۸۲ توسط رابرت کخ (Robert Koch) شناخته و توصیف شد. او موفق به دریافت جایزه نوبل در فیزیولوژی یا پزشکی در سال ۱۹۰۵ برای این کشف شد. کخ (Koch) معتقد نبود که بیماری سل گاومیشی (گاوی) و سل انسانی مشابه باشند. این باور درک اینکه که شیر آلوده هم یک منبع عفونت بود به تعویق انداخت. پس از آن، خطر انتقال از این منبع با اختراع روند پاستوریزاسیون بهطور قابل توجهی کاهش یافت. کخ (Koch) در سال ۱۸۹۰ یک عصاره گلیسیرین از باسیل سل را به عنوان «درمان» سل اعلام کرد. او آن را «توبرکولین» نامید. اگرچه «توبرکولین» مؤثر نبود اما از آن به عنوان یک تست غربالگری برای وجود سل پیش بالینی استفاده شد.
آلبرت کالمیت (Albert Calmette) و کامیل گوئرین (Camille Guérin) در سال ۱۹۰۶ اولین موفقیت را در ایمنسازی علیه سل به دست آوردند. آنها از گونه ضعیفشده سل گاوی استفاده کردند و آن واکسن را BCG نامیدند (باسیل کلمنت و گوئرین). واکسن BCG برای اولین بار در سال ۱۹۲۱ در فرانسه بر روی انسانها مورد استفاده قرار گرفت. با این حال این واکسن BCG پس از جنگ جهانی دوم تنها در USA بریتانیا و آلمان به صورت گسترده پذیرفته شد.
سل به عنوان گستردهترین بیماری همه گیر فقرای شهری، باعث بزرگترین نگرانی عمومی در قرن ۱۹ و اوایل قرن ۲۰ شد. در سال ۱۸۱۵، یکی از هر چهار مرگ در انگلستان به دلیل «سل» بود. در سال ۱۹۱۸، سل دلیل یکی از هر شش مرگ در فرانسه بود. پس از اینکه دانشمندان دهه ۸۰ قرن ۱۹ فهمیدند که بیماری مسری است، سل در فهرست بیماریهای قابل اخطار رسمی در بریتانیا قرار گرفت. کمپینهایی برای جلوگیری از تف کردن مردم در مکانهای عمومی شروع شد و فقرای آلوده به رفتن آسایشگاههایی «تشویق» میشدند که شبیه زندان بود. (آسایشگاهها برای طبقات متوسط و بالا، مراقبتهای عالی و مراقبتهای پزشکی ثابت ارائه میکردند) آسایشگاه ظاهراً مزایای «هوای تازه» و کار ارائه میکردند. اما حتی تحت بهترین شرایط، ۵۰٪ از افرادی که وارد آنجا میشدند ظرف پنج سال فوت میکردند (“ca. ” ۱۹۱۶)
نرخ سل در اروپا، در اوایل قرن ۱۷ شروع به افزایش کرد. سل در اروپا در قرن ۱۸ به اوج خود رسید، زمانی که عامل نزدیک به ۲۵٪ از تمام مرگ و میرها بود. مرگ و میر پس از آن در دهه ۵۰ قرن بیستم نزدیک به ۹۰٪ کاهش یافت. بهبود سلامت عمومی بهطور قابل توجهی میزان سل را حتی قبل از استفاده از استرپتومایسین و آنتیبیوتیکهای دیگر کاهش داد. با این حال، این بیماری یک تهدید قابل توجه برای بهداشت عمومی باقی ماند. هنگامی که شورای تحقیقات پزشکی در انگلستان در سال ۱۹۱۳ تشکیل شد، تمرکز اولیه آن تحقیقات سل بود.
در سال ۱۹۴۶، تولید آنتی بیوتیک استرپتومایسین درمان مؤثر و درمان سل را به یک واقعیت تبدیل کرد. قبل از اینکه این دارو معرفی شود، تنها درمان (به جز آسایشگاهها) مداخله جراحی بود. «روش پنوموتوراکس» ریه آلوده را کلاپس و بیحرکت میکرد تا به آن «استراحت» دهد و امکان درمان ضایعات سلی را فراهم نماید. پیدایش MDR-TB، دوباره جراحی را به عنوان گزینهای از استانداردهای قابلقبول مراقبت در درمان عفونت سل معرفی کرد. مداخلات جراحی کنونی شامل حذف پاتولوژیک حفرههای قفسه سینه («تاول») در ریهها برای کاهش تعداد باکتریها و برای افزایش در معرض دارو قرار گرفتن باکتریهای باقیمانده در جریان خون میباشد. این مداخله بهطور همزمان بار باکتریایی را کاهش میدهد و باعث افزایش اثربخشی درمان آنتیبیوتیک سیستمیک میشود. اگرچه کارشناسان امیدوار بودند سل را بهطور کامل حذف کنند (آبله)، پیدایش گونههای مقاوم در برابر دارو در دهه ۸۰ قرن بیستم حذف سل را غیرمحتملتر کرد. تجدید حیات متعاقب سل موجب اعلام یک وضعیت اضطراری برای بهداشت جهانی توسط WHO در سال ۱۹۹۳ شد.
جامعه و فرهنگ
سازمان بهداشت جهانی و بنیاد بیل و ملیندا گیتس (Bill and Melinda Gates) در حال ارائه کمکهای مالی به تهیه یک آزمون تشخیصی سریع برای استفاده در کشورهایی با درآمد پایین و متوسط هستند. در سال ۲۰۱۱، بسیاری از مکانهای فقیر هنوز هم تنها به میکروسکوپی خلط دسترسی دارند.
در سال ۲۰۱۰، هند بالاترین تعداد کل موارد ابتلا به سل در سراسر جهان را داشت. یکی از دلایل، مدیریت ضعیف این بیماری توسط بخش مراقبتهای بهداشتی خصوصی بود. برنامههایی مانند برنامه کنترل سل ملی اصلاح شده به کاهش میزان سل در میان افرادی که مراقبتهای بهداشتی عمومی دریافت میکنند، کمک میکند.
تحقیقات
واکسن BCG دارای محدودیتهایی است و تحقیق برای تهیه واکسن سل جدید در حال انجام است. چند کاندیدای احتمالی در حال حاضر در فاز I و II کارآزمایی بالینی هستند. دو رویکرد اصلی در حال تلاش برای بهبود اثربخشی واکسن موجود هستند. یک رویکرد شامل اضافه کردن یک واکسن زیرواحد به BCG است. استراتژی دیگر در تلاش برای ایجاد واکسنهای جدید و بهتر است.MVA85A نمونهای از یک واکسن زیرواحد است که در حال حاضر در آفریقای جنوبی در دست آزمایش میباشد. MVA85A مبتنی بر یک ویروس آبله گاوی با اصلاح ژنتیک میباشد. امید است که واکسنها نقش مهمی را در درمان بیماری نهفته و فعال داشته باشند.
برای تشویق کشف بیشتر، محققان و سیاست گذاران، مدلهای جدید اقتصادی توسعه واکسن را ترویج میدهند، از جمله جوایز، مشوقهای مالیاتی و تعهدات بازار پیشرفته. گروههای متعددی در تحقیقات شرکت دارند، از جمله مشارکت توقف سل، ابتکار واکسن سل در آفریقای جنوبی، و بنیاد جهانی واکسن سل Aeras. بنیاد جهانی واکسن سل Aeras هدیهای به مبلغ بیش از ۲۸۰ میلیون دلار (آمریکا) را از بنیاد بیل و ملیندا گیتس به منظور توسعه و تجویز یک واکسن بهبودیافته علیه سل برای استفاده در کشورهای دارای سرایت بالای سل دریافت کرد.
در سایر حیوانات
میکوباکتریها بسیاری از حیوانات مختلف را آلوده میکنند، از جمله پرندگان، جوندگان، و خزندگان. زیرگونه «Mycobacterium tuberculosis» بهندرت در حیوانات وحشی دیده میشود. تلاش برای ریشهکنی سل گاوی ناشی از «میکوباکتریوم بوویس» از گلههای گاو و گوزن نیوزیلند نسبتاً موفق بودهاست. تلاشها در بریتانیا کمتر موفق بودهاند.
پیوند به بیرون
| در ویکیانبار پروندههایی دربارهٔ سل موجود است. |
| |||||||||||
| بیماریهای فقر | |
|---|---|
| بیماریهای مغفول | |
| متفرقه | |
| رشتهها (بیماریزا) بیماریهای عمده |
|
||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|
| افراد مهم | |||||||||||
| موضوعات مرتبط | |||||||||||
| کتابخانههای ملی | |
|---|---|
| سایر | |
|
التهاب مفصل (one joint / a few / پلی آرتریت) |
|
||||||||
|---|---|---|---|---|---|---|---|---|---|
| Other | |||||||||