
تموزولاماید
 | |
 | |
| دادههای بالینی | |
|---|---|
| نامهای تجاری | تمودار، تمودال، تمکد |
| AHFS/Drugs.com | monograph |
| مدلاین پلاس | a601250 |
| دادهها | |
| روش مصرف دارو | خوراکی، داخل وریدی |
| کد ATC | |
| وضعیت قانونی | |
| وضعیت قانونی |
|
| دادههای فارماکوکینتیک | |
| پیوند پروتئینی | ۱۵٪ |
| متابولیسم | در pH فیزیولوژیک بهطور خودبهخود به متابولیتهای تموزولاماید اسید، ۳-متیل-(تریازن-۱-ئیل) ایمیدازول-۴-کاربوکساماید (MTIC) مبدل میشود |
| نیمهعمر حذف | ۱٫۸ ساعت |
| شناسهها | |
| |
| شمارهٔ سیایاس | |
| پابکم CID | |
| IUPHAR/BPS | |
| دراگبنک |
|
| کماسپایدر |
|
| UNII | |
| KEGG |
|
| ChEBI | |
| ChEMBL | |
| CompTox Dashboard (EPA) | |
| ECHA InfoCard | 100.158.652 |
| دادههای فیزیکی و شیمیایی | |
| فرمول شیمیایی | C6H6N6O۲ |
| جرم مولی | 194.151 g/mol g·mol−1 |
| مدل سه بعدی (جیمول) | |
| نقطه ذوب | ۲۱۲ درجه سلسیوس (۴۱۴ درجه فارنهایت) (decomp.) |
| |
| |
|
| |
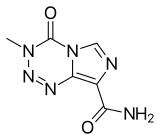
تموزولاماید (انگلیسی: Temozolomide) که با نامهای «تِمودار»، «تِمودال»، «تِمکَد» و «TMZ» هم شناخته میشود، یک داروی شیمیدرمانی خوراکی است.
این دارو که متعلق به خانوادهٔ آلکیله کنندههاست، در درمان برخی از انواع بدخیمیهای مغزی کاربرد دارد: خط اول درمان در گلیوبلاستوم مولتیفرم و خط دوم درمان در «آستروسیتوما» ی مغز.
موارد استفاده
- آستروسیتومای آناپلاستیک مقاوم به داروهای پروکاربازین و نیتروز اوره
- موارد تازهتشخیصدادهشدهٔ گلیوبلاستوم مولتیفرم
عوارض جانبی
شایعترین عارضهٔ جانبی این دارو، ایجاد نارسایی مغز استخوان است. شایعترین عارضهٔ غیرخونی دارو نیز، تهوع و استفراغِ خفیف تا متوسط است که یا خودبهخود متوقف میشود یا نیازمند تجویز داروهای ضد تهوع است. فقط ۴ درصد احتمال دارد که تهوع و استفراغ شدید باشد. در کسانی که به هر دلیل سابقهٔ تهوع و استفراغ دارند، تجویز داروهای ضد تهوع ضرورت مییابد.
این دارو باید با شکم خالی (حداقل یکساعت پیش از غذا) مصرف شود. کپسولها را نباید جوید، بلکه باید با یک لیوان آب قورت داده شوند. داروهای ضد تهوع را هم باید قبل یا حتی همزمان با این دارو مصرف کرد. مصرف این دارو در کسانی که به اجزای سازندهاش یا داروی داکاربازین حساسیت دارند، قدغن است.
تموزولاماید تراتوژن است و اثر سمی بر روی ژنها و همچنین جنین انسان دارد و مصرفش در حاملگی ممنوع است. از آنجایی که این دارو در شیر مادر ترشح میشود، مادران شیردهی که این دارو را مصرف میکنند، نباید به نوزادشان شیر بدهند.
این دارو در مردها هم اثرات سمی بر ژنها دارد و توصیه شده است که مردانی که این دارو را مصرف میکنند، در حین درمان و تا شش ماه پس از خاتمهٔ آن، از تولید مثل و پدرشدن خودداری کنند. بهتر است مردانی که تموزولاماید مصرف میکنند و قصد بچهدار شدن در آینده را دارند، اسپرمشان را قبل از شروع درمان استخراج و در بانک اسپرم نگهداری کنند.
عوارض بسیار نادر این دارو هم شامل «نارسایی تنفس» و «آسیب کبدی» است.
مکانیسم اثر
اثرات درمانی این دارو به توانایی آن در آلکیلدار کردن/متیلدار کردن زنجیرهٔ دیانای بستگی دارد که معمولاً در محلِ نیتروژنِ ۷ (N-7) یا اکسیژنِ ۶ (O-6) بازهایِ گوانین انجام میشود. این متیلدار کردن باعث آسیب DNA و مرگ سلولی میشود. جالب آنکه برخی از تومورها قادرند این آسیب دارویی را ترمیم کنند و به رشدشان ادامه دهند که اینکار را، با ایجاد نوعی آنزیم پروتئینی به نام «او-۶-آلکیلگوانین دیانای آلکیلترانسفراز» انجام میدهند که در بدن انسان توسط ژنی به نام «او-۶-متیلگوانین-دیانای-متیلترانسفراز» (MGMT) کد میشود. برعکس، در برخی تومورها، خاموشسازی اپیژنتیکی این ژن، از ساخت آنزیم مذکور جلوگیری کرده و در نتیجه، این دسته تومورها، بهخوبی به درمان تموزولاماید پاسخ داده و از بین میروند. بدین ترتیب، اگر «پروتئین AGT» در تومور مغزی فردی موجود باشد، این فرد پاسخ چندانی به درمان خاک با تموزولاماید نخواهد داد و عملاً شیمی درمانی با آن فایدهای را در برنخواهد داشت.
خواص شیمیایی
تموزولاماید یک پیشدارو است و مشتقِ ایمیدازوتترازینِ داروی داکاربازین است.
سابقه
این دارو توسط «مالکوم استیونس» و تیمش در «دانشگاه استون» واقع در بیرمنگام انگلستان ساخته شد و از ماه اوت ۱۹۹۹ میلادی در ایالات متحده آمریکا و از همچنین از اوایل دههٔ ۲۰۰۰ میلادی در سایر نقاط جهان در دسترس بوده است.
پژوهشهای جاری
با تکیه بر مشاهدات آزمایشگاهی و کارآزماییهای بالینی، به نظر میرسد که اثرات ضدسرطان تموزولاماید را میتوان با افزودن سایر داروها به آن افزایش داد. به عنوان مثال، کارآزماییهای بالینی نشان داده است که افزودن کلروکین به تموزولاماید، ممکن است اثر بخشی درمان را در بیماران مبتلا به گلیوما افزایش دهد.
برخی مشاهدات آزمایشگاهی حاکی از آن است که افزودن اپیگالوکتشین گالات (یکی از موادِ موجود در چای سبز) به تموزولاماید باعث میشود تا این دارو، با قدرت بیشتری سلولهای سرطانی را بکشد. البته صحت این موضوع تا بهحال، با کارآزمایی بالینی بر روی بیماران مبتلا به تومور مغزی تأیید نشده است.
مطالعات دیگری در سال ۲۰۱۰ میلادی از احتمال سودمند بودنِ نوعی ترکیب جدیدِ افزایشدهندهٔ نفوذپذیری اکسیژن به نام ترانس سدیم کروستین در ترکیب با تموزولاماید و رادیوتراپی خبر دادند و در حال حاضر، یک کارآزمایی بالینی در این مورد در حالِ انجام است.
علاوه بر موارد یادشده و بررسی سودمندی درمان چنددارویی، مطالعات دیگری در حال پیگیری است تا ببیند با تغییر ساختمانی در خودِ مولکول تموزولاماید میتوان قدرت آن را افزایش داد یا خیر. به عنوان مثال مادهٔ طبیعی «پرلیل الکل» را که قبلاً ثابت شده بود اثرات ضدتومور مغزی دارد به مولکول تموزولاماید چسباندند و نتیجهٔ حاصله دارویی شد به نام «TMZ-POH» یا «NEO212» که قدرت ضدسرطانیاش بشدت بالاتر از دو داروی قبلی به تنهایی بود. با آنکه تا سال ۲۰۱۶ میلادی، داروی «NEO212» بر روی انسان آزمایش نشده است، اما در مدلهای حیوانی، خواص درمانیِ ضدسرطانِ فوقالعادهای در مورد «گلیوما»، «ملانوما»، «متاستازهای مغزی» و «سرطان پستان سهمنفی» (سرطان پستانی که رسپتورهای استروژنی، پروژسترونی و HER ندارد) از خود نشان داده است.
از آنجایی برخی تومورها قادرند با بیان ژنی «MGMT»، در مقابل اثرات تموزولاماید مقاومت کنند، پژوهشگران در صددند تا با گنجاندن «او-۶-بنزیلگوانین» (یک مهارکنندهٔ پروتئین آنزیمی AGT) در ساختمان دارو، بر این مقاومت دارویی غلبه کرده و اثرات درمانی آن را افزایش دهند. مطالعات درونکشتگاهی و همچنین درونجانداری در مدلهای حیوانی ثابت کرده است که اینکار واقعاً مؤثر است؛ اما یک کارآزمایی بالینی فاز ۲ که اخیراً بر روی انسان انجام شد، نتایج متفاوت و نامتجانسی در پی داشته است بدین معنی که در بیماران مبتلا به «گلیومای آناپلاستیک مقاوم به تموزولاماید»، اثرات درمانی این دارو افزایش یافت، اما در بیماران مبتلا به «گلیوبلاستوم مولتیفرم مقاوم به تموزولاماید» تأثیر چندانی نداشت.
برخی دانشمندان تلاش میکنند تا با دستکاری ژنتیکی، سلولهای بنیادی خونسازی بسازند که بیانکنندهٔ ژن MGMT باشند و سپس آن را به بیماران مبتلا به تومور مغزی تزریق کنند. بدین ترتیب این بیماران میتوانند دوزهای بیشتری از داروی تموزولاماید را دریافت دارند، بدون آنکه نگران عوارضِ خونی دارو باشند، چرا که سلولهای خونساز به تموزولاماید مقاوم خواهند بود.
دوزهای زیادِ تموزولاماید در بیماران مبتلای به گلیومای درجه بالا، سمیت کمی دارند، اما نتیجه درمان با چنین دوزهایی، همانندِ درمان با دوز معمولی و استانداردِ تموزولاماید بوده است.
- مشارکتکنندگان ویکیپدیا. «Temozolomide». در دانشنامهٔ ویکیپدیای انگلیسی، بازبینیشده در ۹ نوامبر ۲۰۱۶.