
آمیلوئید بتا
| آمیلوئید بتا پپتید (بتا-اِیپیپی) | |||||||||
|---|---|---|---|---|---|---|---|---|---|
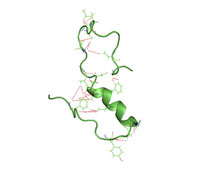 ساختار نیمه چینخوردهٔ آمیلوئید بتا(۱ ۴۰) در یک محیط آبی (pdb 2lfm)
| |||||||||
| شناسهها | |||||||||
| نماد | APP | ||||||||
| پیفم | PF03494 | ||||||||
| اینترپرو | IPR013803 | ||||||||
| SCOPe | 2lfm / SUPFAM | ||||||||
| TCDB | 1.C.50 | ||||||||
| OPM superfamily | 304 | ||||||||
| OPM protein | 2y3k | ||||||||
| Membranome | 45 | ||||||||
| |||||||||
آمیلوئید بتا (انگلیسی: Amyloid beta) که به اختصار Aβ یا Abeta هم گفته میشود، یک پروتئین ۳۶ تا ۴۳ پپتیدی و سازندهٔ اصلی پلاکهای آمیلوئید است که در مغز مبتلایان به بیماری آلزایمر یافت میشود. این پپتیدها از پروتئین پیشساز آمیلوئید-بتا (APP) حاصل میشوند که توسط آنزیمهای بتا سکرتاز ۱ و گاما سکرتاز تجزیه شده و آمیلوئید بتا بهدست میآید. تجمع مولکولهای آمیلوئید بتا، نوعی الیگومر محلولِ انعطافپذیر تشکیل میدهد که به شکلهای گوناگون یافت میشوند. امروزه عقیده بر آن است که برخی اُلیگومرهای بد چینخورده (که به آنها «بذر» یا «ریزدانه» میگویند) مولکولی دیگر آمیلوئید بتا را نیز وادار به چین خوردن نادرست میکنند و یک واکنش زنجیروار پدیدار میگردد که مشابه آن چیزی است که در عفونتهای پریونی دیده میشود. این اُلیگومرها برای یاختههای عصبی سمی هستند. یکی دیگر از پروتئینهای دخیل در ایجاد بیماری آلزایمر هم که پروتئین تاو نام دارد، اُلیگومرهای بد چینخورده شبه پریونی تشکیل میدهد و حتی شواهدی وجود دارد که آمیلوئید بتای بد چینخورده قادر است پروتئین تاو را وادار به تاشدن و چینخوردگی نادرست کند.
طبق پژوهشی در سال ۲۰۱۳، احتمال دارد که خاستگاه پروتئین پیشساز آمیلوئید-بتا بسیار کهن باشد و قدمت آن به دورهٔ نخستین دهاندومیان برسد.
عملکرد
هنوز به درستی معلوم نیست که وظیفهٔ آمیلوئید بتا در بدن چیست. برخی مطالعات حیوانی ثابت کردهاند که فقدان این پروتئین سبب نقص خاصی در عملکرد فیزیولوژیک نمیشود. تا کنون چندین فعالیت بالقوه و احتمالی برای آمیلوئید بتا کشف شده که از جمله میتوان به فعالسازی آنزیم کیناز، محافظت در برابر استرس اکسیداتیو، تنظیم انتقال کلسترول، ایفای نقش بهعنوان فاکتور رونویسی و فعالیت ضد میکروبی (احتمالاً مرتبط با نقش التهابزای این پروتئین) اشاره کرد.
اهمیت بالینی
آمیلوئید بتا سازندهٔ اصلی پلاکهای آمیلوئید است که بهصورت رسوبهای خارجسلولی در مغز مبتلایان به بیماری آلزایمر دیده میشود. آمیلوئید بتا همچنین میتواند باعث ایجاد رسوب در رگهای مغز در جریان آنژیوپاتی مغزی آمیلوئید میگردد. پلاکهای آمیلوئید متشکل از کلافهای از رشتههای منظم است که به آنها «فیبریلهای آمیلوئید» میگویند. این نوع تاشدگی پروتئین در پپتیدهای دیگری همچون پریونها دیده میشوند که مسئول ایجاد بیماریهای ناشی از تاشدگی نادرست پروتئین هستند.
بیماری آلزایمر
تصور پژوهشگران بر آن است که برخی انواع اُلیگومرهای محلول این پپتیدها، عامل بروز بیماری آلزایمر هستند و شدت سمیت اُلیگومرهای آمیلوئید بتا از همه بیشتر است. مطابق فرضیه مجرای یونی در بیماری آلزایمر، اُلیگومرهای محلول غیررشتهای، سبب تشکیل مجراهای یونی میشود که از طریق آنها، کلسیم خودمدار (کلسیمی که تحت نظارت و کنترل سامانههای تنظیمی بدن نیست) به داخل سلولهای عصبی (نرونها) سرازیر میشوند و بدین ترتیب هوموستازی یون کلسیم و متعاقب آن آپوپتوز بههم میریزد. پژوهشهای محاسباتی نشان دادهاست که همچنین پپتیدهای آمیلوئید-بتا که بهصورت مونومرهایی با پیکربندی پیچشی غالب در غشاء سلول تعبیه شدهاند، ممکن است اُلیگومریزه شوند و در نهایت مجراهایی تشکیل دهند که پایداری و ساختار ترکیبی آنها با حضور همزمان و آرایش مولکولی کلسترول در ارتباط است. تعدادی از پژوهشهای ژنتیکی، زیستشناسی سلولی، بیوشیمیایی و مطالعات حیوانی از این فرضیه پشتیبانی میکنند که آمیلوئید-بتا نقشی اساسی در تکوین و ایجاد بیماری آلزایمر دارد.
آمیلوئید-بتای مغز در افراد مبتلا به بیماری آلزایمر غیر ژنتیکی افزایش مییابد. آمیلوئید-بتا ماده اصلی سازنده پارانشیم مغزی و آمیلوئید عروقی است و در ایجاد ضایعات عروقی مغزی مشارکت دارد و برای سلولهای عصبی سمی است. هنوز بهدرستی معلوم نیست این پروتئین چگونه در مغز تجمع یافته و بیماری را آغاز میکند. برخی از پژوهشگران دریافتهاند که الیگومرهای آمیلوئید-بتا برخی از نشانههای بیماری آلزایمر را از طریق رقابت با انسولین جهت اتصال به گیرنده آن القا میکنند و بنابراین متابولیسم گلوکز در مغز را مختل میکنند. تلاشهای فراوانی برای درک مکانیسمهای تولید آمیلوئید-بتا شدهاست، از جمله تحقیق بر روی آنزیمهای پروتئولیتیک گاما سکرتاز و بتا سکرتاز که سبب تشکیل آمیلوئید-بتا از پروتئین پیشساز آن، پروتئین پیشساز آمیلوئید (APP) میگردد. آمیلوئید-بتا در پلاسما، مایع مغزی نخاعی (CSF) و مایع بینبافتی مغز (ISF) بهطور عمده به صورت مولکول محلول Aβ۴۰ گردش مییابد. پلاکهای آمیلوئید مغز هر دو نوع پروتئین Aβ۴۰ و Aβ۴۲ را دارند، در حالی که آمیلوئید عروقی، عمدتاً دارای نوع کوتاهتر Aβ۴۰ هستند. چندین توالی مختلف آمیلوئید-بتا در هر دو ضایعه (مغزی و عروقی) یافت شدهاست. احتمال دارد تولید آمیلوئید-بتا در دستگاه عصبی مرکزی بهدنبال انتقال آکسونی بتا سکرتاز و پرسنیلین-۱ با واسطه پروتئین پیشساز آمیلوئید، در غشای آکسونی عصبی صورت گیرد.
افزایش در سطح کلی آمیلوئید-بتا یا غلظت نسبی هر دو مولکول Aβ۴۰ و Aβ۴۲ (که اولی بیشتر در پلاکهای عروق مغزی و دومی در پلاکهای عصبی متمرکز است) در پاتوژنز بیماری آلزایمر خانوادگی و غیر خانوادگی نقش دارند. به دلیل ماهیت آبگریز، مولکول Aβ۴۲ آمیلوئیدوژنیکترین شکل پپتید است. با این حال، مشخص شده که توالی مرکزی KLVFFAE به تنهایی قادر به تشکیل آمیلوئید است و احتمالاً هسته فیبریل را تشکیل میدهد. یک پژوهش دیگر، سطح Aβ۴۲ در مغز را هم با شروع بیماری آلزایمر و هم با کاهش فشار مایع مغزی نخاعی مرتبط میداند، و این موضوع نشان میدهد که تجمع یا ناتوانی در پاکسازی قطعات Aβ۴۲ احتمالاً در بیماریزایی آلزایمر نقش داشته باشد.
بیشتر پژوهشگران «فرضیهٔ آمیلوئید» (که میگوید پلاکهای آمیلوئیدی مسئول ایجاد آلزایمر هستند) را قبول دارند، اما این فرضیه بهطور قطعی اثبات نشدهاست. یک فرضیه دیگر بیان میدارد که الیگومرهای آمیلوئید (و نه پلاکهای آن) سبب ایجاد آلزایمر میشوند. موشهایی که برای بیان الیگومرها (و نه پلاکها) دستکاری ژنتیکی شدهاند (APPE693Q) به آلزایمر مبتلا میشوند. علاوه بر این، احتمال ابتلا به آلزایمر در موشهایی که برای تبدیل الیگومرها به پلاک مهندسی ژنتیک شدهاند (APPE693Q X PS1ΔE9)، بیشتر از موشهای الیگومری نیست. رسوبات درون سلولی پروتئین تاو نیز در آلزایمر مشاهده شدهاست، و همچنین ممکن است تجمع آلفا-سینوکلئین در ایجاد آلزایمر مؤثر باشد.
سرطان
با آنکه بهنظر میرسد آمیلوئید بتا در ایجاد سرطان نقش داشته باشد، تحقیقات اخیر در مورد انواع سرطانها جهت روشن کردن ماهیت اثرات احتمالی آن، نتایج غیرقابل اتکایی داشتهاست. سطح آمیلوئید بتا در برخی سرطانها همچون سرطان مری، سرطان روده بزرگ، سرطان ریه و سرطان کبد ارزیابی شدهاست، چرا که مشاهده شده در کسانی که از این سرطانها جان سالم بدر میبرند، احتمال بروز آلزایمر کم است. در تمامی این سرطانها، رابطهٔ مثبتی با افزایش سطح آمیلوئید بتا مشاهده شده، بهویژه در سرطانهای کبد. با این حال سمت و سوی این رابطه هنوز معلوم نیست. پژوهشهای مربوط به سلولهای سرطان پستان در انسان نشان داده که بیان پروتئین پیشساز آمیلوئید-بتا در این سلولها افزایش یافتهاست.
نشانگان داون
در بزرگسالان مبتلا به نشانگان داون تجمع آمیلوئید در ارتباط با بیماری آلزایمرشان دیده شده که با افت عملکرد شناختی، حافظه، حرکات ظریف، کارکرد اجرایی و مهارتهای بینایی-فضایی در ارتباط است.
- مشارکتکنندگان ویکیپدیا. «Amyloid beta». در دانشنامهٔ ویکیپدیای انگلیسی، بازبینیشده در ۹ ژوئن ۲۰۲۱.